La produzione di idrogeno attraverso idrolisi termica

acqua-migliore.com
Articolo a cura di Ulderico DI CAPRIO
L’idrogeno è il miglior candidato ad essere il combustibile del domani. Infatti, può essere prodotto attraverso vari processi. Molti dei quali utilizzano fonti rinnovabili sia per l’apporto di energia, che per le materie prime. L’idrolisi termica dell’acqua è una di queste. Tale processo è molto versatile, in quanto sfrutta l’acqua e qualsiasi tra le fonti energetiche: nucleare, fossile o solare.
Idrolisi termica: dall’acqua all’idrogeno
Alla base di questa tecnica di produzione di idrogeno, c’è la reazione inversa alla produzione dell’acqua. L’acqua è l’unico reagente di tale reazione e porta alla produzione di idrogeno molecolare e ossigeno molecolare.
2H2O⇌2H2+O2
Tale reazione avviene oltre i 3000°C. L’idrogeno è un ottimo combustibile e l’ossigeno è un comburente, ciò li porta a ricombinarsi e rilasciare, molto velocemente, l’energia immagazzinata. Considerando quando appena detto, tale questa tecnica non sembra molto promettente, anzi è controproducente, a causa delle elevate temperature richieste, e molto pericolosa, a causa delle esplosioni. Come rendere questa reazione fattibile e sicura? Bisogna trovare qualcosa che innalzi la capacità dell’acqua di dividersi e che allo stesso tempo non faccia incontrare idrogeno ed ossigeno. La soluzione è utilizzare un materiale in grado di assorbire e rilasciare ossigeno in una reazione ciclica.
Come avviene la reazione?
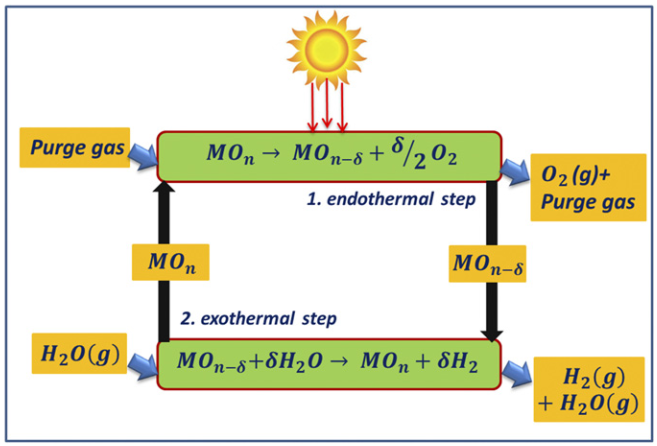
Tale compito viene svolto da sostanze capaci di accumulare ossigeno e rilasciarlo “su richiesta”. La reazione globale viene quindi divisa in due parti.
- Nella prima il materiale “assorbe” l’ossigeno della molecola d’acqua facendo formare idrogeno. Questa prima reazione (ossidazione) è endotermica (ovvero richiede un apporto di energia per avvenire).
- Il materiale ossidato è successivamente recuperato in una seconda reazione dove viene rilasciato l’ossigeno (riduzione). Tale reazione è esotermica (ovvero rilascia energia quando avviene). Per aumentare l’efficienza del ciclo di reazioni si alterano le temperature e le pressioni.
L’ossidazione avviene a temperature e pressioni elevate (che dipendono dal materiale scelto), per favorire cinetica e termodinamica. La riduzione avviene a temperature a pressioni più basse rispetto alla prima, in quanto così l’allontanamento di idrogeno è favorito.
Quali sono i materiali che permettono questa reazione?
La produzione di idrogeno con idrolisi termochimica richiede un materiale che abbia sia buone capacità riduttive che ossidative. La sfida nello sviluppo di questo processo sta proprio nel trovare tale materiale. I migliori a svolgere questo compito sono ossidi di ferro, miscele solide di ossidi di cerio e zirconio e perovskite. Tutti questi materiali hanno mostrato ottime capacità di accumulo e rilascio di ossigeno.
I migliori risultati si stanno avendo con perovskiti artificiali (formula generale ABO). Il sito A ospita una miscela di lantanio e stronzio mente nel sito B si usa una miscela mista di manganese e ferro. Attraverso il sito B è possibile modulare la capacità di riduzione e ossidazione del materiale. Attraverso tali proprietà è possibile identificare e settare i parametri con i quali condurre il processo.
